- Hvad er et atom?
- Hvordan er et atom opbygget?
- Hvordan kombineres atomer?
- Dele af et atom
- Historien om atomet
- Molekyle
Vi forklarer, hvad et atom er, og hvordan hver af dets dele er opbygget. Også dens historie, undersøgelser om det og hvad et molekyle er.

Hvad er et atom?
Den mindste enhed, der udgør stof.
Ordet atom kommer fra oldgræsk (atom, "Uden opdeling") og blev opfundet af de første filosoffer til at teoretisere om sammensætningen af ting, det vil sige de elementære partikler i univers. Siden da, med fremkomsten af atommodeller, måden at forestille sig dem på har varieret enormt, da en atommodel afløste den forrige gennem århundrederne, indtil vi nåede den, vi bruger i dag.
Atomer har egenskaber som kemisk element der komponerer og til gengæld er elementerne organiseret og klassificeret efter deres atomnumre, elektronisk konfiguration og kemiske egenskaber i Periodiske system af elementerne.
Det samme kemiske grundstof kan være sammensat af forskellige atomer af samme klasse, det vil sige med samme atomnummer (antal protoner som hvert atom har i grundstoffet), selvom deres atommasse er forskellige.
For eksempel er der forskellige atomer af det samme grundstof, der adskiller sig i deres antal neutroner, og de kaldes isotoper, er et repræsentativt tilfælde isotoper af grundstoffet kulstof (12C, 13C, 14C). Så hvert atom tilhører det samme kemiske element eller ej, afhængigt af dets antal protoner, så atomer med det samme antal protoner tilhører det samme kemiske element.
Hvordan er et atom opbygget?
Atomer er opbygget af en kerne og en eller flere elektroner (som har en negativ ladning) omkring den. Kernen består af partikler kaldet protoner og neutroner. Protoner er positivt ladede og neutroner er neutrale. Sættet af protoner og neutroner kaldes nukleoner.
Protoner og elektroner tiltrækkes af hinanden af den elektromagnetiske kraft (samspillet mellem ladede partikler og elektriske og magnetiske felter), mens protoner og neutroner tiltrækkes af hinanden af kernekraften (en kraft, der kun opleves af de partikler, der udgør atomkerne).
Hvordan kombineres atomer?
Atomer kan kombineres med hinanden og dannes kemiske forbindelser, hvad sker der, når de deler deres elektroner på den ene eller anden måde. Kemiske bindinger kan være kovalent, ionisk Y metallisk, som stammer fra kovalente molekylære forbindelser, ioniske netværk eller metalliske forbindelser (selvom det er vigtigt at præcisere, at ingen kemisk binding er absolut kovalent eller ionisk). På denne måde kan atomer kombineres og dannes molekyler simpelt som Vand, samt at danne makromolekyler kompleks lignende protein, DNA Y RNA.
Selvom atomer adskiller sig fra hinanden takket være konfigurationen af deres partikler, er det også rigtigt, at alle atomerne i det samme grundstof er nøjagtigt identiske: brintatomerne i Sol De er de samme som dem, der udgør vores krop, og kulstofatomerne i en hunds krop er identiske med dem, der udgør en diamant. Forskellen ligger i den måde, hvorpå atomerne kombineres til at udgøre de forskellige kemiske forbindelser, der udgør organerne og organsystemerne i levende væsner, materialerne genereret i industri, og alt det stof, der udgør universet.
Dele af et atom
Atomer er opbygget af to væsentlige dele:
- Kernen. Omkring 99,94% af massen af et atom er koncentreret i kernen, hvor protonerne og neutronerne (som tilsammen kaldes "nukleoner") er forbundet af stærke kernekræfter, som forhindrer protonerne i at frastøde hinanden, at have samme elektriske oplade.
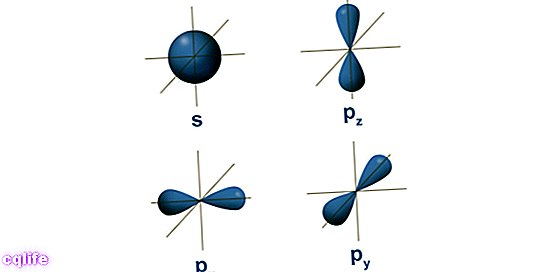
- De atomare orbitaler. En orbital beskriver et område af rummet, der omgiver atomkernen, hvori sandsynlighed at finde en elektron er meget høj. Disse områder har forskellige former, der opnås som et resultat af løsning af den stationære Schrödinger-ligning. Erwin Schrödinger var en østrigsk videnskabsmand, der udviklede denne ligning i 1925 for at beregne udviklingen af en subatomær partikel, såsom elektroner. Elektronerne danner således en slags "sky" omkring kernen, som er repræsenteret ved atomorbitalernes form. På den anden side svarer hver atomorbital til en bestemt energiværdi for elektroner, så de er organiseret efter deres energiværdier. Følgende figur viser formerne af de første atomare orbitaler:
Historien om atomet

Den første til at formulere ideen om eksistensen af atomer var den græske filosof Demokrit (s.V-VI f.Kr.) ud fra rent imaginære spekulationer (som videnskaben blev forstået på det tidspunkt).
Hans studier blev taget op af senere filosoffer som Leucippus og Epicurus, men det blev forsømt under middelalderlige, overskygget af den kreationistiske forklaring af verden, som tilskrev alt til Gud.
Vi måtte vente til 1773, da den franske kemiker Antoine de Lavoisier postulerede sin teori om ikke-skabelse eller ødelæggelse af stof (det forvandler sig kun) eller Lov om bevarelse af masse, som gjorde det muligt for John Dalton at formulere den første moderne atomteori i 1804.
Successive lærde af fysisk og kemi de var inspireret af hans arbejde med at foreslå bedre og mere komplekse systemer til at forstå de grundlæggende partikler af stof. Efterfølgende blev der foreslået nye atommodeller op til de mest brugte i dag.
Den nutidige accepterede struktur er den, der stammer fra eksperimenter af Rutherford i 1911, sammen med formuleringerne af Niels Bohr, Schrödinger og Heisenberg.
Molekyle
Et molekyle er kendt som foreningen af to eller flere atomer gennem kemiske bindinger for at danne en mere kompleks og elektrisk neutral struktur. Kemiske bindinger kan være kovalente eller ioniske.
Molekyler kan bestå af atomer af det samme kemiske grundstof, for eksempel oxygenmolekylet (O2), eller af atomer af forskellige kemiske grundstoffer, for eksempel glucosemolekylet. Monatomiske gasser, for eksempel helium (He), betragtes også som molekyler.

