- Hvad er kulbrinter?
- Karakteristika for kulbrinter
- Klassificering af kulbrinter
- Betydningen af kulbrinter
- Derivater og anvendelser af kulbrinter
- Kulbrinters miljøpåvirkning
Vi forklarer, hvad kulbrinter er, deres egenskaber og hvordan de klassificeres. Hertil kommer dets derivater, applikationer og miljøpåvirkning.

Hvad er kulbrinter?
Kulbrinter er forskellige typer forbindelser økologisk. De kan have en større eller mindre kompleksitet, men de er altid opbygget af et skelet af atomer kulstof (C) og brint (H), samt andre evt elementer.
Hver kulbrinte præsenterer sine strukturelle mønstre, da dens specifikke konfiguration bestemmer dens fysiske og kemiske egenskaber, samt navnet på stof hvad det handler om. Det Petroleum, det naturgas og kul er de vigtigste kilder til kulbrinter.
De fleste af kulbrinterne er i det indre af jorden, begravet under lag og lag af sten og Jeg plejer. De er produktet af den anaerobe nedbrydning, under meget specifikke forhold, af store mængder af organisk materiale, som i oldtiden udgjorde kroppen af forskellige levende væsner.
Kulbrinter er også til stede i kroppen af forskellige levende væsener, under specifikke former, såsom gummiet, som gummitræer genererer, eller et sæt pigmenter kaldet carotener, som nogle planter har. Derudover kan de syntetiseres i et laboratorium, der regner med Råmateriale tilstrækkelig.
På grund af deres enorme kemiske og energimæssige potentiale er kulbrinter en uundværlig del af forskellige industrierblandt dem ved at opnå elektrisk strøm.
Karakteristika for kulbrinter
Nogle karakteristika ved kulbrinter er:
- De består for det meste af kulstof og brint, og eventuelle tilsætningsstoffer af andre grundstoffer eller andre radikale grupper. Mens deres kulstofatomer udgør strukturen af forbindelsen, tjener brint i nogle tilfælde som en bro til at holde dem sammen i en konfiguration (form, struktur, orientering) bestemt.
- De kan have en ramme af molekyler lineær eller forgrenet, åben eller lukket. Det afhænger af dens bestilling og mængde af komponenter, om det er et eller andet kulbrinte.
- De er meget brandfarlige og har en enorm energikapacitet, hvilket gør dem til et ideelt råmateriale til industriel transformation og til at opnå energi.
- De er for det meste giftige og kan udsendes dampe farlig for Sundhed.
Klassificering af kulbrinter
Siden deres opdagelse i det 19. århundrede er kulbrinter blevet klassificeret efter to mulige kriterier: deres type struktur og typerne af bindinger mellem deres atomer. Ifølge den første klassifikation skelnes der mellem to kategorier:
- Acykliske eller åben kæde kulbrinter. Det er dem, hvis kæde af molekyler ikke lukker sig om sig selv. Til gengæld kan de opdeles i lineære (linjeformede) eller forgrenede (med forskellige grene). For eksempel:
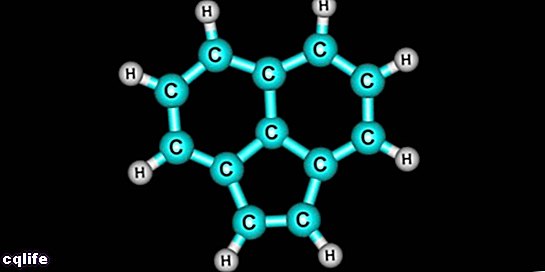
- Cykliske eller lukkede kulbrinter. De er dem, hvis kæde af molekyler lukker om sig selv. Til gengæld kan de opdeles i monocykliske (enkeltcyklus) og polycykliske (flere cyklusser). For eksempel:
Ved at adlyde den anden klassifikation har vi i stedet:
- Aromatiske kulbrinter. De har en aromatisk ring, det vil sige en cyklisk struktur, der adlyder den såkaldte Hückel-regel, som siger, at antallet af delokaliserede elektroner i en aromatisk forbindelse overholder:
Hvor:
-
- n. Repræsenterer en helt tal.
- Ne. Repræsenterer antallet af elektroner delokaliseret i den aromatiske forbindelse.
For eksempel har benzen (C6H6) 6 delokaliserede elektroner (kaldet pi (𝛑) elektroner) i sin struktur, hvilket indebærer, at n skal være lig med 1.
Næsten alle aromatiske kulbrinter er normalt afledt af benzen (selvom ikke altid), og derfor er den sekskantede struktur af benzen en del af mange af disse aromatiske forbindelser. Navnet "aromatisk" kommer fra det faktum, at disse forbindelser oprindeligt blev opnået ved nedbrydning kemiske stoffer behagelig lugt. Nogle eksempler på aromatiske forbindelser er:
- Alifatiske kulbrinter. De mangler en aromatisk ring. Dens navn kommer fra græsk aliphar, det vil sige "fedt", da de blev opnået ved nedbrydning af olier og fedtstoffer. De er klassificeret som mættede (udrustet med enkeltatombindinger) og umættede (besidder mindst én multipel-, dobbelt- eller tredobbeltbinding). Nogle eksempler på alifatiske kulbrinter er:
Betydningen af kulbrinter
Kulbrinter er ekstremt alsidige stoffer, da de tjener som Råmateriale at få meget varierede produkter. Derudover har de et stort energipotentiale, det vil sige deres forbrænding er let og intens, så de energisk opretholder et mangfoldigt sæt af industrierlige fra materialer, opløsningsmidler, det fossile brændstoffer, til generering af elektrisk energi.
Dertil kommer det faktum, at deres dannelse tog millioner af år med langsomme kemiske processer under jorden, så de udgør en vigtig ressource, men kan ikke fornyes, som en dag vil være udmattet for altid (eller i det mindste i et godt stykke tid). Dets brug bør finde sted under forhold med ekstremt ansvar.
Derivater og anvendelser af kulbrinter

Kulbrinter har et stort sæt anvendelser til menneske, blandt hvilke skiller sig ud:
- Strømproduktion. Takket være dens enorme kapacitet til forbrænding, kulbrinter anvendes som strømkilde At generere elektricitet. Dette udføres i visse typer kraftværker og leverer energi til både boliger og andre industrier og tillader understøttelse af vores livsstil.
- Generering af brændstoffer. Deres energikapacitet giver dem mulighed for at fremstille forskellige typer brændstoffer (benzin, diesel, naturgas flydende), til at drive forskellige typer køretøjer eller til at drive forskellige husholdningsapparater såsom rumvarmere, komfurer og varmeapparater, der fungerer ved hjælp af gasser såsom butan eller propan.
- Indhentning plastik. Forskellige typer plast og alsidige materialer kan fås i laboratorier fra håndtering af kulbrinter. Disse materialer er så billige, effektive og enkle at fremstille, at der er en enorm industri omkring dem.
- Fremstilling af opløsningsmidler og andre Produkter. Mange kulbrinter er væsentlige komponenter i opløsningsmidler og opløsningsmidler, rengøringsmidler, gødning eller bitumen.
Kulbrinters miljøpåvirkning
Brugen af kulbrinter har sine omkostninger, og den første indvirkning han tager den miljø. Generelt handler det om giftige stoffer, der er i stand til at producere store økologiske skader i tilfælde af, at de bliver dumpet i natur, som ved olieudslip eller olielækager. Reparation af disse miljøskader er ofte dyrt og tidskrævende.
Hertil kommer, afhængigt af kulbrinte, dets frigivelse eller dets forbrænding udsender gasser af drivhuseffekt til atmosfære, det vil sige gasser rige på kulstof såsom metan (CH4) eller carbondioxid (CO2).
Disse gasser kan ødelægge ozonlag planeten, og blokerer også for energiudslip gennem atmosfæren, hvilket dramatisk bidrager til global opvarmning og til klima forandring. Afbrænding af fossile brændstoffer er faktisk en af hovedfaktorerne i dette globale problem.
