Adenosinmonophosphat er et nukleotid, der kan repræsentere en del af energibæreren adenosintrifosfat (ATP). Som et cyklisk adenosinmonophosphat fungerer det også som en anden messenger. Det oprettes blandt andet, når ATP nedbrydes, hvilket frigiver energi.
Hvad er adenosinmonophosphat?
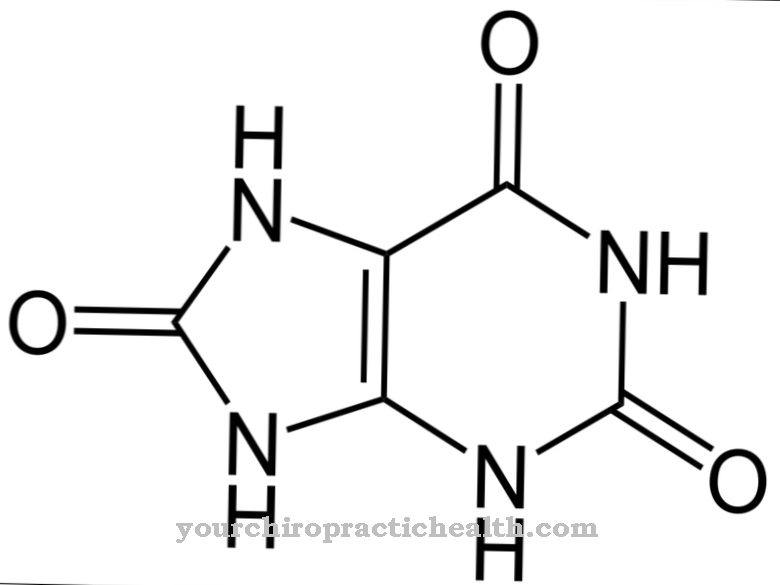
Adenosinmonophosphat (C10H14N5O7P) er et nukleotid og hører til purinribotiderne. Purin er et byggemateriale i den menneskelige krop, der også findes i alle andre levende ting. Molekylet danner en dobbeltring og vises aldrig alene: Purin er altid knyttet til andre molekyler for at danne større enheder.
Purine er en af byggestenene til adenin. Denne base findes også i deoxyribonucleic acid (DNA) og koder genetisk lagret information. Ud over adenin hører guanin også til purinbaserne. Adeninet i adenosinmonophosphat er knyttet til to andre byggesten: ribose og fosforsyre. Ribose er et sukker med den molekylære formel C5H10O5. Biologi kalder også molekylet pentose, fordi det består af en fem-leddet ring. I adenosinmonophosphat binder fosforsyre sig til det femte carbonatom i ribose. Andre navne på adenosinmonophosphat er adenylat og adenylsyre.
Funktion, effekt og opgaver
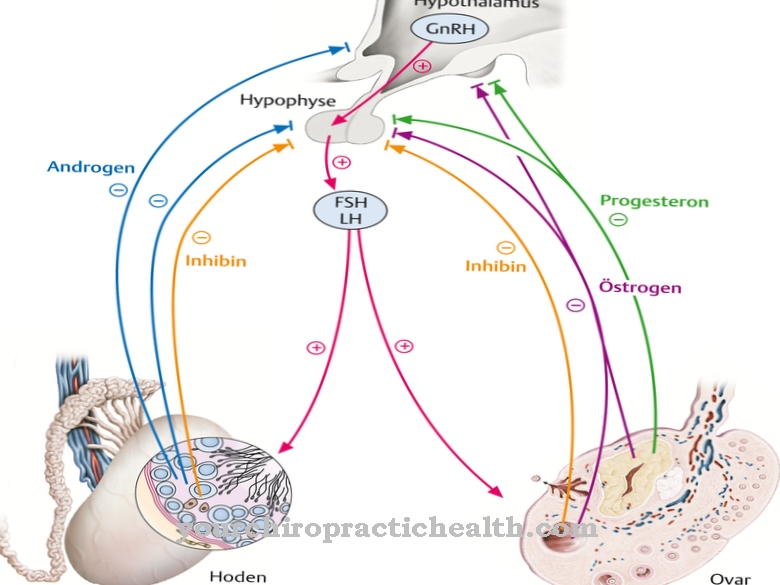
Cyklisk adenosinmonophosphat (cAMP) understøtter transmission af hormonelle signaler. Et steroidhormon binder for eksempel til en receptor, der er placeret på ydersiden af cellemembranen. På en måde er receptoren cellens første modtager. Hormonet og receptoren passer sammen som en nøgle og lås og udløser således en biokemisk reaktion i cellen.
I dette tilfælde er hormonet den første messenger, der aktiverer enzymet adenylatcyklase. Denne biokatalysator opdeler nu ATP i cellen og skaber cAMP. Derefter aktiverer cAMP igen et andet enzym, der afhængigt af celletypen udløser cellens respons - for eksempel produktion af et nyt hormon. Adenosinmonophosphat har funktionen af dit andet signalstof eller en anden messenger.
Antallet af molekyler forbliver imidlertid ikke det samme fra trin til trin: Antallet af molekyler øges cirka ti gange pr. Reaktionstrin, hvilket øger cellens respons. Dette er også grunden til, at hormoner er tilstrækkelige i meget lave koncentrationer til at udløse en stærk reaktion. Ved afslutningen af reaktionen er alt, der er tilbage af cAMP, adenosinmonophosphat, som andre enzymer kan vende tilbage til cyklussen.
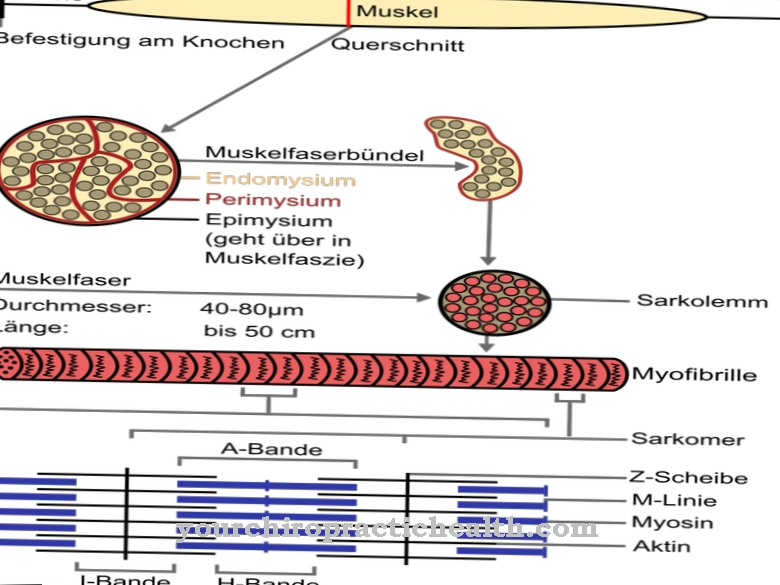
Når et enzym opdeler AMP fra adenosintrifosfat (ATP), genereres der energi. Den menneskelige krop gør forskellige anvendelser af denne energi. ATP er den vigtigste energibærer inden for levende væsener og sikrer, at biokemiske processer kan finde sted på mikroniveau såvel som muskelbevægelser.
Adenosinmonophosphat er også en af byggestenene til ribonukleinsyre (RNA). I kernen til menneskelige celler opbevares genetisk information i form af DNA. Så at cellen kan arbejde med den, kopierer den DNA'et og opretter et RNA. DNA og RNA indeholder den samme information om det samme afsnit, men adskiller sig i strukturen af deres molekyler.
Uddannelse, forekomst, egenskaber & optimale værdier
Adenosinmonophosphat kan opstå fra adenosintrifosfat (ATP). Enzymet adenylat cyclase opdeler ATP og frigiver energi i processen. Stoffernes fosforsyre spiller en særlig vigtig rolle. Fosfoanhydritbindinger kobler de individuelle molekyler til hinanden. Spaltning kan have adskillige mulige resultater: enten enzymer opdeler ATP i adenosindiphosphat (ADP) og orthophosphat eller i AMP og pyrophosphat. Da energimetabolismen i det væsentlige er som en cyklus, kan enzymer også kombinere de individuelle byggesten tilbage til ATP.
Mitokondrierne er ansvarlige for syntesen af ATP. Mitochondria er celleorganeller, der fungerer som cellernes kraftstationer. De adskilles fra resten af cellen ved hjælp af deres egen membran. Mitochondria er arvet fra moderen (moderen). Adenosinmonophosphat forekommer i alle celler og kan derfor findes overalt i den menneskelige krop.
Sygdomme og lidelser
En række problemer kan opstå med adenosinmonophosphat. F.eks. Kan syntesen af ATP i mitochondria forstyrres. Medicin kalder også en sådan dysfunktion mitokondrisk sygdom. Det kan have en række forskellige årsager, herunder stress, dårlig kost, forgiftning, skader på frie radikaler, kronisk betændelse, infektion og tarmsygdom.
Genetiske defekter er ofte ansvarlige for udviklingen af syndromet. Mutationer ændrer den genetiske kode og fører til forskellige lidelser i energimetabolismen eller i molekylers struktur. Disse mutationer findes ikke nødvendigvis i cellekernens DNA; Mitochondria har deres egen genetiske sammensætning, der findes uafhængigt af cellekernens DNA.
Ved mitokondriopati producerer mitokondrierne kun ATP langsommere; cellerne har derfor mindre energi. I stedet for at bygge komplet ATP syntetiserer mitokondrierne mere ADP end normalt. Cellerne kan også bruge ADP til energiproduktion, men ADP udsender mindre energi end ATP. Ved mitokondrisk sygdom kan kroppen bruge glukose som en energileverandør; når de nedbrydes, produceres mælkesyre. Mitokondrisk sygdom er ikke en sygdom i sig selv, men er et syndrom, der kan være en del af en sygdom.
Medicin opsummerer forskellige manifestationer af mitokondriske lidelser under navnet. Det kan for eksempel forekomme i forbindelse med MELAS-syndromet. Dette er en neurologisk sygdom, der er kendetegnet ved anfald, hjerneskade og en øget dannelse af mælkesyre. Derudover er mitokondrisk sygdom også relateret til forskellige former for demens.













.jpg)